تاثیر فشار و ناخالصی روی نقطه جوش، ذوب و انجماد
فشار بخار:
مولکول های یک مایع دارای انرژی جنبشی هستند و انرژی جنبشی مولکول معینی از یک مایع ضمن برخورد با سایر مولکول ها دائماً تغییر می کند. در یک لحظه معین تعدادی از مولکول ها دارای انرژی نسبتاً زیاد و تعدادی دارای انرژی نسبتاً کمی هستند. مولکول هایی که انرژی جنبشی آن ها زیاد است می توانند بر نیروی جاذبه مولکول های اطراف خود غلبه کرده و از سطح مایع فرار کرده و وارد فاز گازی شوند.
چگونگی جوشیدن مایع:
وقتی فشار بخار یک مایع با فشار جو برابر می شود مایع شروع به جوشیدن می کند. در این دما بخار حاصل در داخل مایع سبب ایجاد حباب و غلیان خاص جوشش می شود.
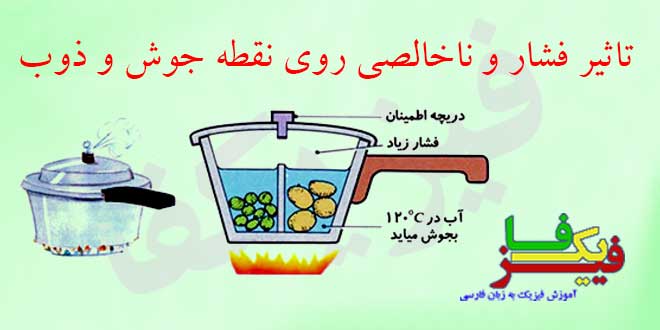
نقطه جوش یک مایع با تغییر فشار خارجی تغییر می کند. افزایش فشار باعث افزایش نقطه جوش و کاهش فشار باعث کاهش نقطه جوش میشود. به طور مثال در ارتفاعات، آب در دمای پایینتری به جوش می آید. نوسانات فشار جو در یک موقعیت جغرافیایی نقطه جوش آب را حداکثر تا ۲ درجه سانتیگراد تغییر می دهد ولی تغییر محل ممکن است باعث تغییرات بیشتر شود.

متوسط فشاری که هواسنج در سطح دریا نشان می دهد، یک اتمسفر ولی در ارتفاعات بالاتر کمتر از این مقدار است. مثلاً در ارتفاع ۵۰۰۰ پایی از سطح دریا متوسط فشاری که فشارسنج نشان می دهد ۰٫۸۳۶ اتمسفر است و نقطه جوش آب در این فشار ۹۵٫۱ درجه سانتیگراد می باشد.
اثر ناخالصی در نقطهی جوش :

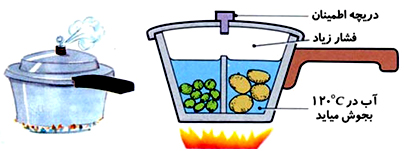
اثر ناخالصی باعث افزایش نقطه ی جوش می شود زیرا با ناخالصی مایع دیرتر جوش می آید. برای مثال در تابستان ها برای اینکه آب رادیاتور دیرتر جوش بیاید در آب آن کمی ضد جوش می ریزند که این کار موجب می شود آب دیر تر جوش بیاید و به ماشین آسیب نرسد. به عنوان مثال افزایش نمک در آب باعث افزایش نقطه جوش آن می شود و بدین ترتیب می توان نقطه جوش آب را به بالای ۱۰۰ درجه افزایش داد.
اثرناخالصی روی نقطه جوش دو حالت دارد :
۱) اگر ناخالصی غیرفرار باشد (مانند نمک) همواره نقطه جوش را بالا می برد.
۲) اگر ناخالصی فرار باشد (مانند الکل) گاهی باعث افزایش و گاهی باعث کاهش نقطه جوش می شود.
نقطه ذوب:
نقطه ذوب یکی از خواص فیزیکی اجسام به شمار می رود و درجه حرارتی است که در آن درجه جسم جامد به مایع تبدیل می شود یا به عبارت دیگر درجه حرارتی است که در آن درجه فشار بخار جامد با فشار بخار مایع برابر است. در واقع ذوب تغییر از ترتیب خیلی منظم ذرات در شبکه کریستالی به ترتیب خیلی اتفاقی که مشخصه یک مایع است میباشد. وقتی که درجه حرارت به حدی می رسد که در آن انرژی حرارتی ذرات به نیروهای درون کریستالی فائق شود جسم شروع به ذوب شدن می کند.
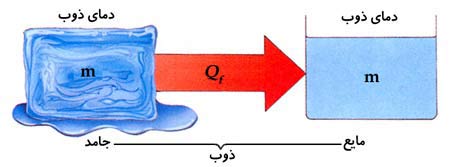
در مورد ترکیبات غیر یونی نقطه ذوب پایین است زیرا نیروهای بین مولکولی در مقایسه با نیروهای بین یونی ضعیف می باشند. در درجه حرارت ذوب حالت جامد و حالت مایع جسم با هم در حال تعادل هستند و برای یک جسم خالص در تمام مدت ذوب درجه حرارت ثابت می باشد. هنگامی که به جسم جامد حرارت داده می شود افزایش حرارت باعث بالا رفتن درجه حرارت آن می شود تا اینکه اولین ذره آن ذوب شود از این لحظه به بعد گرمای داده شده صرف ذوب شدن جسم جامد می شود و تا آخرین ذره جسم جامد باقی است، درجه حرارت بالا نمی رود که این درجه حرارت ذوب می باشد.
اگر حرارت دور شود درجه حرارت پایین نمی آید تا این که تمام مایع به جامد تبدیل شود( منجمد شود). بنابراین نقطه ذوب و نقطه انجماد یک جسم خالص یکسان است. پس از ذوب کامل اگر حرارت دادن را ادامه دهیم مایع شروع به گرم شدن می کند تا به نقطه جوش برسد و در آن نقطه نیز تا آخرین قطره مایع باقی است درجه حرارت نقطه جوش ثابت می ماند.
تاثیر فشار اتمسفر روی نقطه ذوب:
تاثیر فشار اتمسفر روی نقطه ذوب بسیار جزئی می باشد. زیرا اگرچه افزایش فشار ذرات جامد را به یکدیگر نزدیک می کند و به این ترتیب نیروی بین مولکولی افزایش می یابد و بنابراین دمایی که برای جدا کردن مولکول ها لازم است کمی بیشتر می شود. ولی چون ذرات جامد در هر صورت به هم نزدیک هستند و قابلیت تراکم چندان زیادی ندارند، تغییر فشار خارجی نمی تواند تغییر زیادی در نقطه ذوب جامدات بدهد و به استثنای بعضی از مواد مثل یخ افزایش فشار، نقطه ذوب بیشتر جامدات را کمی افزایش می دهد که البته در مورد یخ افزایش فشار سبب کاهش نقطه ذوب آن می شود.
تاثیر ناخالصی روی نقطه ذوب:
وجود ناخالصی معمولا نقطه ذوب جسم را پایین می آورد و مخلوط دو ماده مختلف دارای نقطه ذوب پایین تری از هر کدام از این دو ماده است. اگر چنانچه دو ماده دارای نقطه ذوب یکسانی باشند و مخلوط این دو ماده نیز دارای همان نقطه ذوب باشند می توان نتیجه گرفت که این دو ماده یکی هستند. به طور کلی از نزول نقطه ذوب که در اثر ناخالصی در یک ترکیب به وجود می آید، می توان برای شناسایی و پی بردن به وجود ناخالصی استفاده نمود.
نقطه انجماد:
وقتی یک مایع را به اندازه کافی سرد کنیم، به جامد تبدیل می شود. تبدیل شدن مایع به جامد را انجماد میگویند. دمایی که در آن ماده ی مایع به جامد تبدیل می شود، نقطه انجماد نامیده می شود.

بعضی از مواد، مثل یخ، در یک دمای معین از حالت جامد به حالت مایع در می آیند و قبل از ذوب شدن نرم نمی شوند. اگر این گونه مواد را سرد کنیم، در همان دمایی که ذوب شده اند، به حالت جامد در می آیند. موادی مانند یخ، قلع و سرب از این دسته موادند. این مواد دارای نقطه ذوب معین هستند. یعنی دقیقاً می توانیم بگوییم که این مواد در چه دمایی ذوب (یا منجمد) می شوند. در این گروه از مواد نقطه ی ذوب با نقطه ی انجماد برابر است.
گروهی دیگر از مواد در هنگام تبدیل از حالت جامد به مایع کم کم نرم می شوند. مثلاً قیر و شیشه وقتی گرم شوند ابتدا نرم می شوند و از حالت جامد خارج می گردند، سپس در اثر گرم شدن بیشتر، کم کم به طور کامل به حالت مایع در می آیند، این گونه مواد نقطه ی ذوب معینی ندارند و اصطلاحاً گفته می شود که این مواد ذوب خمیری دادند. موادی که دارای نقطه ی ذوب معینی هستند، نقطه ی انجماد می توانند به حالت جامد یا مایع یا به هر دو حالت وجود داشته باشند.
اثر ناخالصی در نقطه انجماد :
ناخالصی سبب کاهش نقطه ی انجماد می شود. در زمستان ها برای آن که آب داخل رادیاتور یخ نزند در آن ماده ایی به نام ضد یخ می ریزند که باعث می شود آب داخل رادیاتور یخ نبندد یا دیرتر یخ ببندد ضدیخ از مایعی شبیه الکل و آب مخلوط می شود.




24 دیدگاه دربارهٔ «تاثیر فشار و ناخالصی روی نقطه جوش، ذوب و انجماد»
ممنون از سایت خوبتون اگه میشه تاثیر فشار بر نقطه ی انجماد رو نیز بذارید?
نقطه ذوب و نقطه انجماد یکسان هستند
سلام ببخشید میشه علت اینکه تاثیر فشار بر نقطه ذوب یخ برعکس دیگر موارد هس رو بگین؟
برمیگرده به ساختار مولکولی آب در دماهایی که تبدیل به جامد می شود.
سلام جناب کبیری، خداقوت..برای امتحان های مجازی دوران کرونایی در جستجوی تعداد زیادی سوال بودم تا بتوانم از هریک از دانش آموزان با سوال منحصر به خودش امتحان بگیرم، سایت شما کمک زیادی کرد. داشتن معلمان جوان و پرانرژی و با وسعت قلبی مثل شما که به رایگان نتیجه زحمات خودرا در اختیار دیگران قرار می دهند، باعث دلگرمی و خوشحالی ماست.
خوشحالم از اینکه توانستم کمکی کرده باشم. سپاس از لطف و محبت شما
:/
سلام استاد مطالب عالی بود ازتون ممنونم
سپاس
سلام خسته نباشید واقعا ممنونم، خیلی کامل و واضح بود
سپاس
سلام استاد ببخشید میشه روی زودپز مثال بزنید چرا افزایش فشار باعث افزایش نقطه جوش میشه
بسیار عالی است واقعا هرکاری کردم نمیتوانستم بفهمم تا اینکه جزوه شما رو خوندم. شما در کدام شهر هستید؟
ممنونم
همکلاسی سابق سلام
موفقیتت همیشگی🌹
سلامت باشی
سلام و سپاس از لطفت. همچنین برای شما هم موفقیت روز افزون و سلامتی آرزو می کنم.
سلام خداقوت
یک سوال داشتم ؛چرا هوا باعث افزایش نقطه ذوب می شود ؟
ذوب شذن یعنی افزایش فاصله بین مولکول های جامد. که در نهایت پس از ذوب تبدیل به مایع میشه. ولی اینکه منظور سوال شما افزایش هوا بود یا افزایش فشار هوا نمی دونم؟ لطفا سوال خود را دقیق بپرسید.
یه سوال داشتم خواستم بپرسم ماده ای هست که باعث شه نقطه انجماد آب بیشتر بشه
اگر امکانش هست هر دو رو بفرمایید
هم افزایش هوا و هم فشار هوا .
ممنون
افزایش فشار هوا باعث میشه مولکول ها، سخت تر فاصله اشون زیاد شه. برای همین نیاز به دماهای بالاتری داریم تا فاصله مولکول ها زیاد شه. در نتیجه نقطه ذوب افزایش پیدا میکنه.
خیلی ممنون
سپاس
سلام چرا تاثیر ناخالصی توی نقطه ذوب
بیشتر است ؟
ناخالصی یعنی اضافه شدن اتم های جدید به اتم های قبلی. اینکار باعث می شود پیوند های قوی تری بین اتم ها شکل گیرد. در نتیجه برای جدا کردن آن ها از یکدیگر باید گرمای بیشتری بدهیم. در نتیجه نقطه جوش افزایش می یابد.