جامدات شکل مشخصی دارند. دلیل اینکه مولکول های این مواد در کنار یکدیگر قرار دارند و یک شکل را ساختند، وجود نیرویی است که این مولکول ها را در کنار هم نگه می دارد. این نیرو از طرف مولکولهای همسایه ی مولکول در ماده، وارد می شود و مثل فنری مولکولهای مجاور را به هم وصل کرده است. به این نیرو، نیروی بین مولکولی می گوییم.
در مایعات هم نیروی بین مولکولی وجود دارد و مولکول ها در کنار هم یک حجم از مایع را می سازند که این حجم برای ما قابل مشاهده است. اگر نیروهای بین مولکولی در مایعات وجود نداشتند، مولکول های مایع مثل مولکول های گاز در فضا پراکنده بودند و چون مولکول ها آنقدر کوچک هستند که با چشم ما قابل مشاهده نیستند، ما قادر به مشاهده مواد مایع نبودیم. نیروی بین مولکولی باعث می شود تعداد زیادی از مولکول های یک ماده در کنار هم قرار بگیرند و حجم مشخصی از آن ماده را بسازند تا ما بتوانیم آن را مشاهده کنیم.
در نظر بگیرید که مولکول های یخ، آب و بخار هوا (حالت های مختلف ماده)، هر سه H2O هستند اما ما شکل مایع و جامد آب را می بینیم اما شکل گاز آب را به خاطر پراکنده بودن مولکول ها نمی توانیم ببینیم.
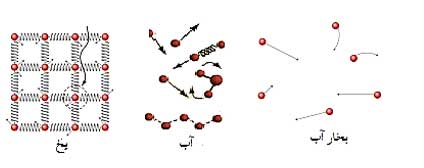
نیروی بین مولکولی
نیروهای بین مولکولی خیلی مهم اند چون تعیین کننده خواص فیزیکی مولکول ها مثل نقطه جوش آنها، نقطه ذوب و … است. این نیروها مانند فنر در بین مولکول ها عمل می کنند یعنی اگر فاصله بین مولکول ها خیلی کم شود، مانند حالتی که فنر جمع می شود، نیرویی به سمت بیرون به مولکول مجاور وارد می شود تا دو مولکول از هم دور شوند. و اگر فاصله دو مولکول خیلی زیاد شود، مانند حالتی که فنر باز شده است، نیرویی به سمت داخل به مولکول مجاور وارد می شود تا فاصله را کمتر کند. مانند شکل زیر.
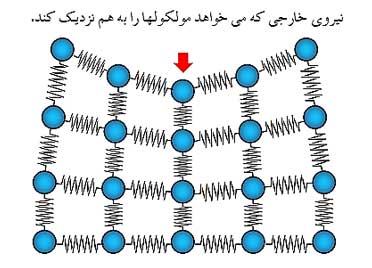
در آزمایش سرنگ در بخش قبل دیدیم که حجم مایع را نمی توانیم با فشرده کردن کم کنیم. زیرا نیروهای بین مولکولی مانند شکل بالا عمل می کنند و نمیگذارند که مولکولها بیش از حد به هم نزدیک شوند.
نیروی هم چسبی و دگر چسبی
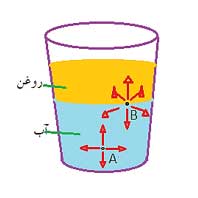
اکنون لیوانی بردارید و در آن مقداری روغن و مقداری آب بریزید. به مولکول های آب در نقطه A نیرو هایی از طرف دیگر مولکول های آب که در همسایگی اش قرار دارند، وارد می شود. چون این نیرو بین مولکول های همسان وجود دارد، به این نیروها، نیروی هم چسبی گفته می شود. توجه داشته باشید که نیروهای بین مولکولی کوتاه برد هستند یعنی اگر فاصله دو مولکول بیشتر از حدی باشد، دیگر این دو مولکول، نیرویی به هم وارد نمی کنند پس به علت کوتاه برد بودن نیروی بین مولکولی، مولکول های روغن که در همسایگی مولکول A نیستند، به این مولکول نیرویی وارد نمی کنند.

حال مولکول Bدر سطح آب و روغن را در نظر بگیرید. به مولکول B نیرویی از طرف مولکول های آب مجاور و نیرویی از طرف مولکول های روغن وارد می شود. به نیرویی که بین مولکول های روغن و مولکول های سطحی آب وارد می شود، دگر چسبی می گویند چون این نیرو بین مولکول های با دو جنس متفاوت وجود دارد.
مثال ۱:
وقتی شیشه می شکند، با نزدیک کردن قطعه های آن به هم نمی توان اجزای شیشه را دوباره به هم چسباند؛ ولی اگر قطعه های شیشه را آنقدر گرم کنیم که نرم شوند، می توان آنها را به هم چسباند. با توجه به کوتاه برد بودن نیروهای بین مولکولی توجیه کنید.
پاسخ:
وقتی دو قطعه شیشه را به هم نزدیک می کنیم، فاصله مولکول های دو قسمت شکسته شده، آنقدر زیاد است که نمی توانند به یکدیگر نیرو وارد کنند. اما اگر شیشه را گرم کنیم تا نرم شود، انرژی مولکول ها و حرکتشان بیشتر می شود و می توانند به هم نزدیک تر شوند. بنابر این به هم نیروی هم چسبی وارد میکنند و می چسبند.
مثال ۲:
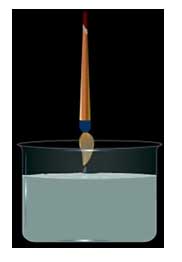
وقتی قلم موی خشکی را نگاه می کنیم مشاهده می کنیم که موهای آن با فاصله از هم قرار گرفته است. اما وقتی آن را در آب خیس کنیم، میبینیم که به هم می چسبند. دلیل این پدیده را توضیح دهید.

پاسخ:
وقتی که قلم مو را خیس می کنیم و از آب خارج می کنیم، به علت نیروی هم چسبی بین مولکول های آب، این لایه های آب که بین موهای قلم مو قرار گرفته است، به هم می چسبند و بنابر این مشاهده می کنیم که موهای قلم مو به هم نزدیک می شوند.
کشش سطحی
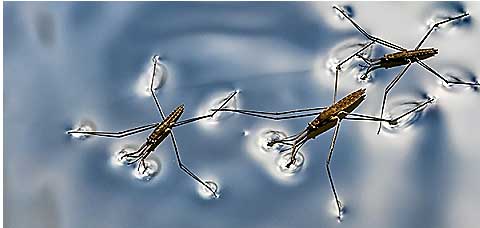
لیوانی را پر از آب کنید و یک سوزن را با دقت روی سطح آب قرار دهید. می بینیم که سوزن روی آب می ماند و غرق نمی شود.

حال لیوان دیگری را پر از آب کنید و یک قطعه یخ را در آن قرار دهید. یخ روی آب می ماند. حال با انگشت یخ و سوزن را به پایین فشار دهید.
می بینیم که سوزن به ته لیوان می رود و غرق می شود اما یخ دوباره به سطح لیوان برمی گردد. دلیل این اتفاق این است که چگالی یخ کمتر از آب است بنابر این روی آب باقی می ماند اما چگالی سوزن بیشتر از آب است و در آب غرق می شود. اما چرا در ابتدا سوزن با این که چگالی بیشتری داشت توانست روی آب باقی بماند؟
علت این پدیده این است که سطح آب مثل یک تشک نرم رفتار می کند. اگر جسم سبکی روی آن قرار بگیرد، مثل یک تشک، کمی خم می شود ولی جسم را بر روی خودش نگه می دارد. به این پدیده کشش سطحی می گویند.
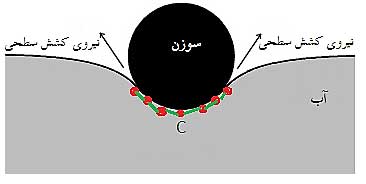
کشش سطحی نیرویی است که بین مولکول های سطح یک مایع و مولکول های مجاور وجود دارد. اگر جسم سبکی به آرامی روی سطح مایع قرار بگیرد،(مانند شکل زیر) به مولکول C از مایع که زیر جسم قرار دارد نیرویی از طرف مولکول های مجاور وارد می شود. مولکول های مجاور سعی می کنند تا پیوند بین خود و مولکول C را حفظ کنند بنابر این کمی فاصله بین مولکول C و همسایگانش بیشتر می شود چون کمی پایین تر می رود اما پیوند بینشان شکسته نمی شود.اما در صورتی که جسم سنگین باشد یا نیرویی وارد کنیم که از نیروی بین مولکولی مولکول های سطح مایع بیشتر باشد، پیوند ها شکسته می شوند، مولکول C به یک طرف می چسبد و راه برای جسم برای سقوط در مایع باز می شود و جسم در آب غرق می شود.
به همین دلیل است یک پشه می تواند روی آب راه برود ولی شما نمی توانید روی آب راه بروید.
مثال ۳:
سعی کنید یک سوزن را مطابق شکل روی سطح آب شناور کنید. پس از شناور شدن، سطح آب را به دقت مشاهده کنید. چه می بینید؟

اکنون یکی دو قطره مایع شوینده به آرامی به آب درون ظرف بیفزایید. چه اتفاقی می افتد؟ چرا؟
پاسخ:
در ابتدا می بینیم که با قرار دادن سوزن روی آب، سطح آب مثل یک تشک فرو رفته است اما بعد از اضافه کردن مایع ظرفشویی می بینیم که سوزن غرق می شود. دلیل این پدیده این است که اضافه کردن مایع ظرفشویی باعث می شود که نیروی همچسبی بین مولکول های آب کم شود. بنابر این کشش سطحی کم می شود وسطح مایع توانایی نگه داشتن سوزن بر روی خود را از دست میدهد.
پاورپوینت تدریس ویژگی های ماده را به دبیران گرامی پیشنهاد میکنیم.
چرا قطره آب کروی است؟
درون یک قطره ی آب، هرمولکول آب توسط مولکول های همسایه جذب می شوند. چون این نیروها با هم برابر و در جهت مخالف هستند، با هم خنثی می شوند و مولکول حرکت نمی کند. اما به مولکول های سطح قطره فقط نیرویی از طرف مولکول های داخل قطره و مولکول های مجاور در سطح قطره وارد می شود و نیرویی به این مولکولها از سمت خارج وارد نمیشود. نیروهایی که از طرف مولکولهای مجاور وارد می شود با هم خنثی می شوند.
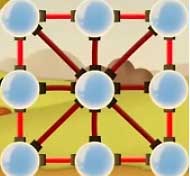
بنابر این به هر مولکول در سطح یک نیروی خالص به سمت مرکز وارد می شود. این نیرو سعی می کند تا جایی که می تواند مولکول ها را به مرکز نزدیک کند. بنابر این مولکول هایی که در فاصله های دورتر از مرکز قرار دارند، توسط این نیروها به مرکز نزدیک می شوند. مانند شکل:
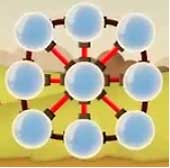
بنابر این مولکول ها سعی می کنند به هم نزدیک تر شوند تا بتوانند به مرکز نزدیک تر شوند. در بین شکل ها کمترین مساحت را کره دارد. یعنی اگر n مولکول در سطح مایع داشته باشیم،اگر این تعداد در مساحت کمتری قرار بگیرند، فاصله شان از هم کمتر می شود و به مرکز نزدیک تر می شوند.

مثال ۴:
شکل روبرو خروج قطره های روغن با دمای متفاوت را از دهانه دو قطره چکان نشان می دهد.

الف) توضیح دهید در کدام شکل دمای قطره روغن کمتر است.
ب) افزایش دما چه تاثیری بر نیروی همچسبی مولکول های یک مایع می گذارد؟
پ) چرا هنگام شستن ظروف، افزون بر استفاده از مایع ظرفشویی، ترجیح می دهیم از آب گرم نیز استفاده کنیم؟
پاسخ:
الف) هر چه دما بیشتر باشد، انرژی مولکول ها و سرعت حرکتشان بیشتر می شود بنابر این نیروی هم چسبی بین مولکول ها کاهش می یابد. و هر چه دما کمتر باشد، نیروی همچسبی بیشتر می شود و قطرات مایع برای اینکه بر این نیروی همچسبی غلبه کنند و از دیگر مولکول های مایع داخل قطره چکان جدا شوند، باید وزن بیشتری داشته باشند تا نیروی گرانش وارد شده بتواند بر نیروی همچسبی غلبه کند. بنابر این روغن سمت چپ سردتر است.
ب)افزایش دما باعث افزایش انرژی مولکول ها و سرعت حرکتشان می شود بنابراین نیروی هم چسبی بین مولکول ها کاهش می یابد.
پ)در آب گرم، نیروی همچسبی بین مولکولهای آب کمتر می شود بنابر این راحت تر می توانند به مواد دیگر بچسبند. به عبارت دیگر، نیروی دگرچسبی مولکول های مواد دیگر و آب به راحتی می تواند بر نیروی همچسبی مولکولهای آب غلبه کند بنابر این قطرات آب به راحتی به اجسام دیگر می چسبند و آلودگی ها را به خود جذب می کنند و ظرف ها تمیز می شوند.
تر شوندگی

دو سطح شیشه ای در دست بگیرید. روی یکی از آنها را با روغن چرب کنید. حال با قطره چکان روی هر کدام از آنها یک قطره آب بچکانید. چه مشاهده می کنید؟ روی کدام سطح، قطره آب بیشتر پخش شد؟
سطح شیشه ای که چرب شده بود، اصطلاحا تر شوندگی کمتر و آب گریزی بیشتری داشت. و سطح دیگر آب گریزی کمتر و تر شوندگی بیشتری داشت. مقدار آب گریزی و تر شوندگی سطوح را با زاویه ای که قطره با سطح می سازد تعیین و مقایسه می کنند. این زاویه به نیروهایی که از مولکولهای داخل قطره به هم وارد می کنند (نیروی همچسبی) و نیرویی که مولکولهای سطح به مولکول های مایع وارد می کند(نیروی دگر چسبی) بستگی دارد. هرچه این زاویه به صفر نزدیک تر باشد، می گویند میزان تر شوندگی بیشتر است و هرچه بیشتر شود و به ۱۸۰ نزدیکتر باشد می گویند میزان آب گریزی بیشتر است. زاویه تماس، مستقل از اندازه و شکل مولکول و حجم قطره است.
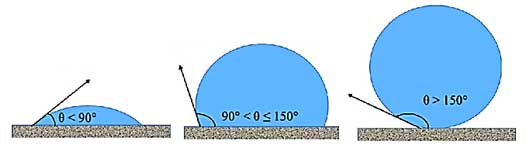
اگر نیروی هم چسبی مولکول های مایع از نیروی دگر چسبی بین مولکول های مایع و سطح بیشتر باشد، به مولکول های سطح نیرویی بیشتری از طرف مولکول های داخل قطره وارد می شود و قطره تمایل دارد تا شکل کروی خود را حفظ کند و به سطح نمی چسبد و سطح را تر نمی کند.
مثال ۵:
الف) یک طرف یک تکه شیشه ی کوچک را کمی بالاتر از شعله یک شمع بگیرید تا سطح شیشه به طور کامل دوداندود شود. شیشه را از طرف تمیز آن روی سطحی افقی قرار دهید و سپس روی سطح دود اندود شده ی آن چند قطره آب بریزید. دلیل آنچه را مشاهده می کنید توضیح دهید.
ب) بار دیگر سطح شیشه را به جای دود اندود کردن، با روغن چرب کنید و آزمایش را تکرار کنید. نتیجه را توضیح دهید.
ج) چرا آب روی گلبرگ ها و برگ های نیلوفر آبی، به صورت قطره های ریز و درشت در می آیند؟
پاسخ:
الف) اگر روی شیشه تمیز مقداری آب بریزیم، آب شیشه را تر می کند اما آب نمی تواند سطح دوده اندود شیشه را تر کند. چون نیروی همچسبی بین مولکول های آب از نیروی دگر چسبی بین مولکول های آب و دوده بیشتر است و آب به شکل قطره های کروی کوچک روی سطح قرار می گیرد.
ب) مانند حالت بالا، چون نیروی دگر چسبی بین مولکول های آب و روغن از نیروی هم چسبی بین مولکول های آب کمتر است، مولکول های آب جذب روغن نمی شوند و به یکدیگر می چسبند بنابر این به شکل قطره کروی آب روی سطح باقی می مانند.
ج) چون نیروی هم چسبی بین مولکول های آب از نیروی دگر چسبی بین مولکول آب و برگ نیلوفر بیشتر است، مولکولهای آب به مولکولهای برگ نمی چسبند و توسط دیگر مولکولهای آب جذب می شوند و شکل کروی ایجاد می کنند.
مثال ۶:
الف) مطابق شکل زیر، کارت را طوری روی لبه لیوان قرار دهید که تنها نیمی از آن با آب در تماس باشد. وزن های چند گرمی را روی قسمتی از کارت که با آب در تماس نیست قرار دهید.(ابتدا وزنه ۵ گرمی، سپس ۱۰ گرمی و…) نتیجه مشاهدات را توضیح دهید.

ب) یکی دو قطره مایع شوینده به آب اضافه کنید و آزمایش را تکرار کنید. نتیجه مشاهدات خود را بگویید.
پاسخ:
الف)وقتی وزنه سبک اضافه می کنیم مشاهده می شود که کارت از سطح اولیه خود کمی بالاتر می آید و سطح آب در تماس خود را نیز کمی بالا می برد. علت این پدیده این است که نیروی دگر چسبی بین مولکول های آب و کارت از نیروی همچسبی بین مولکول های آب بیشتر است. بنابر این نیروی دگر چسبی غلبه می کند و باعث می شود مولکول های آب کمی دور شوند. اما وقتی وزنه سنگین می شود، نیروی وزن آنها بیشتر از نیروی دگر چسبی بین مولکولهای کارت و آب می شود و مولکول های کارت از مولکول های آب جدا می شوند.
ب) در این حالت، با افزودن مایع شوینده، با قرار دادن وزنه ها، کارت به راحتی از آب جدا می شود. علت این است که مایع شوینده باعث می شود که نیروی دگر چسبی بین مولکولهای کارت و آب کاهش یابد.
پیشنهاد می کنیم مطلب اثر مویینگی را حتما مشاهده کنید.
ویدیو آموزشی نیروی بین مولکولی
در این ویدیو که توسط استاد مصطفی کبیری آماده شده است، با نیروهای هم چسبی و دگر چسبی و کشش سطحی آشنا می شوید. همچنین ماهیت هر یک از این نیروها را می آموزید.
مشاهده در یوتیوب | مشاهده در آپارات



13 دیدگاه دربارهٔ «نیروی بین مولکولی»
سلام مطالب خیلی مفید و کاملی بود واقعا خسته نباشید
سپاس
عالی بود یک دنیا ممنون
خیلی کامل و مفید بود خیلی ممنونم
سپاس
عالی👏
سلام خسته نباشید،وقتتون بخیر
اگه امکانش هست به ۲ سوال بنده پاسخ بدید ممنون میشم
۱.تمام عوامل موثر بر نیروی بین مولکولی؟
۲.تاثیر ناخالصی ها بر روی نیروی بین مولکولی نیروی بین مولکولی را زیاد میکند یا کم؟
هم چسبی بود نیروی بین دو مولکول همسان
دگری چسبی بود نیروی بین دو مولکول از دو ماده مختلف
بعد چرا وقتی آب و میریزیم تو یک استوانه یا مثلا یک لوله مویین
دگرچسبی که بیشتره
کشش سطحی داریم مگه کشش سطحی مال همچسبی نیست؟
اینو متوجه نمیشم میشه توضیح بدید .
عامل کشش سطحی نیروی هم چسبی بین مولکول های سطح مایع است. مویینگی از برایند نیروهای دگر چسبی (بین شیشه و آب) و هم چسبی (مولکول های آب) حاصل میشه. دگرچسبی بیشتر از هم چسبی میشه پس یک سطح کاو ایجاد می شود. لطفا جزوه مویینگی را در لینک زیر مشاهدخ کنید:
https://physicfa.ir/اثر-مویینگی/
عالی بود خیلی ممنون از سایت خوبتون
سپاس از لطف شما
خیلی ممنون… خیلی کامل و جامع بود🤝🏼
سپاس