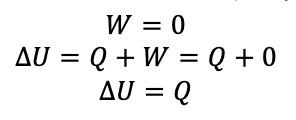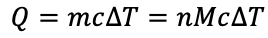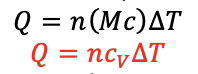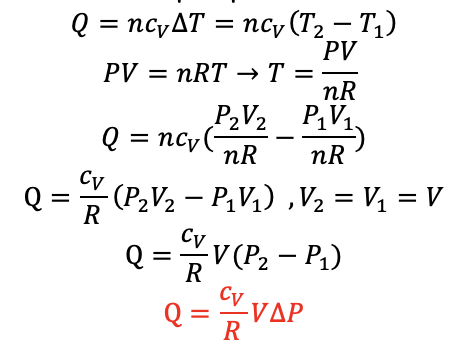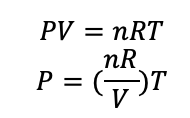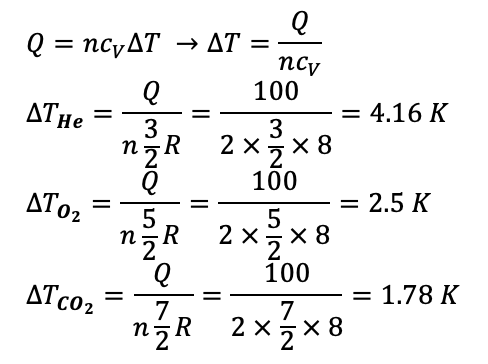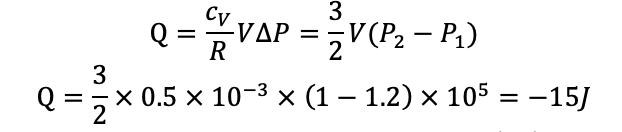دستگاه های ترمودینامیکی می توانند فرایندهای مختلفی را طی کنند. در بین این فرایند ها، فرایندهای خاصی وجود دارند که کاربرد آنها وسیع تر است. از جمله فرایند هم حجم ، فرایند هم فشار ، فرایند هم دما و فرایند بی دررو . در ادامه این مطلب به توصیف فرایند هم حجم می پردازیم.
فرایند هم حجم
همانطوری که از نام فرایند مشخص است، حجم گاز در طی این فرایند ثابت می ماند و از آن جایی که می دانیم تا تغییر حجم صورت نگیرد، کاری صورت نمی گیرد، بنابراین در فرایند هم حجم کار صفر است.
در این فرایند، گاز با محیط فقط تبادل گرما می کند و تغییر انرژی درونی گاز با توجه به قانون اول ترمودینامیک، برابر با گرمایی است که با محیط (منبع گرما) مبادله می شود.
گرما
با توجه به رابطه گرما می توان به صورت زیر فرمول گرما در فرایند هم حجم را حساب کرد.
می دانیم جرم گاز برابر m=nM است که M جرم مولی گاز است. می توان حاصلضرب دو ثابت جرم مولی و گرمای ویژه را با ثابت دیگری بنام گرمای ویژه مولی در حجم ثابت نشان داد.
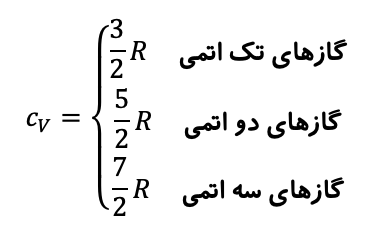
مقدار گرمای ویژه مولی در حجم ثابت را می توان برای گاز های مختلف با تقریب مناسبی به صورت زیر در نظر گرفت.
می توان رابطه زیر را نیز برای محاسبه گرما در این فرایند با استفاده از معادله حالت ،اثبات کرد.
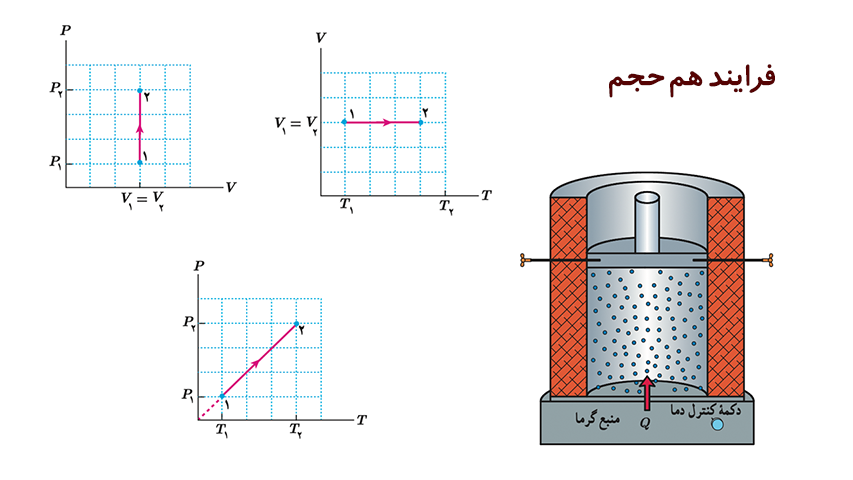
نمودارهای فرایند هم حجم
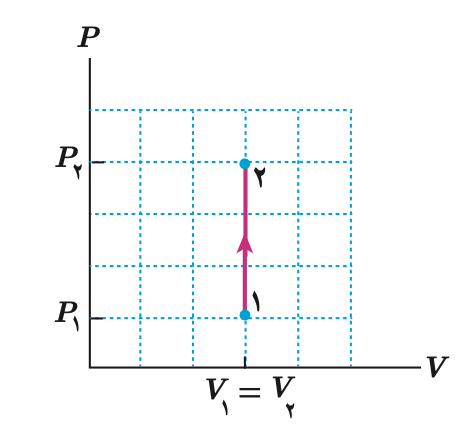
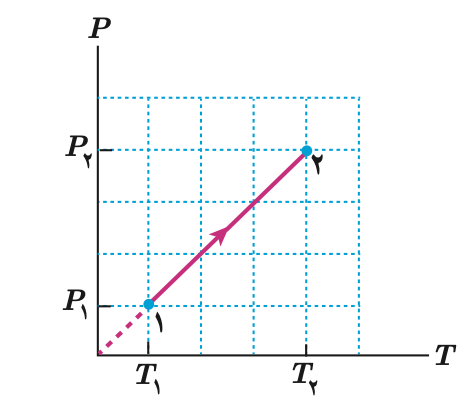
با توجه به معادله حالت می توان به صورت زیر رابطه بین فشار و دمای گاز را بدست آورد که معادله یک خط راست است که از مبدا نمودار P-T می گذرد.
اگر در فرایند هم حجم دمای گاز را کاهش دهیم، فشار گاز نیز کاهش می یابد و در نمودارهای بالا، جهت را برعکس رسم می کنیم.
مثال ها
مثال ۱: روی قوطی های افشانه (اسپری)، هشدار داده شده است که از انداختن آن در آتش خودداری کنید.علت این توصیه چیست؟
پاسخ: با داغ شدن قوطی، جنبش مولکول های گاز زیاد شده و فشار وارد از گاز به دیواره های ظرف افزایش می یابد و این می تواند موجب ترکیدن قوطی شود. این نمونه ای از یک فرایند هم حجم است که در آن افزایش دما و فشار گاز در حجم ثابت اتفاق می افتد.
مثال ۲: به ۲ مول از گازهای آرمانی He,O2,CO2 در حجم ثابت ۱۰۰ ژول گرما می دهیم. دمای هر یک تقریباچقدر افزایش می یابد؟
پاسخ:
پاسخ: برای گاز تک اتمی خواهیم داشت.
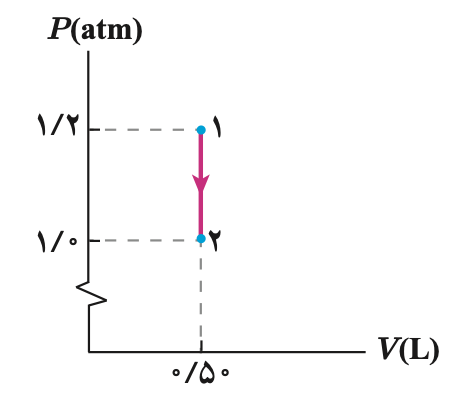
یعنی گاز ۱۵ ژول گرما از دست داده است.
مثال ۴: دمای n مول گاز با گرمای ویژه مولی در حجم ثابت CV در یک فرایند هم حجم از T1 به T2 رسیده است.
الف) تغییر انرژی درونی گاز در این فرایند را بیابید.
ب) اگر این گاز، گاز آرمانی و تک اتمی باشد ، تغییر انرژی درونی آن به چه صورتی نوشته می شود؟
پاسخ: الف)در حجم ثابت ، کار صفر است. بنابراین:

برای طرح مثال های بیشتر نیاز داریم تا فرایند های دیگر را نیز بیاموزیم. چون که در مثال ها چند فرایند مختلف داریم. برای مشاهده مثال های بیشتر به این مطلب مراجعه کنید.
ویدیو آموزشی
در ویدیو آموزشی زیر به بررسی ویژگی ها و روابط و نمودارهای این فرایند توسط استاد مصطفی کبیری، پرداخته می شود.
مشاهده در یوتیوب | مشاهده در آپارات