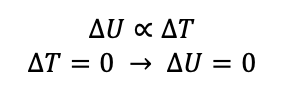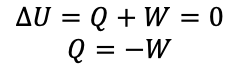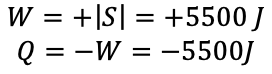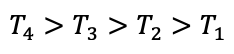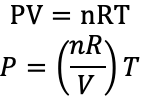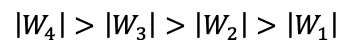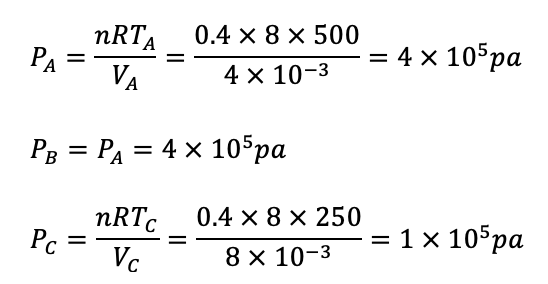دستگاه های ترمودینامیکی می توانند فرایندهای مختلفی را طی کنند. در بین این فرایند ها، فرایندهای خاصی وجود دارند که کاربرد آنها وسیع تر است. از جمله فرایند هم حجم ، فرایند هم فشار ، فرایند هم دما و فرایند بی دررو . در ادامه این مطلب به توصیف فرایند هم دما می پردازیم.
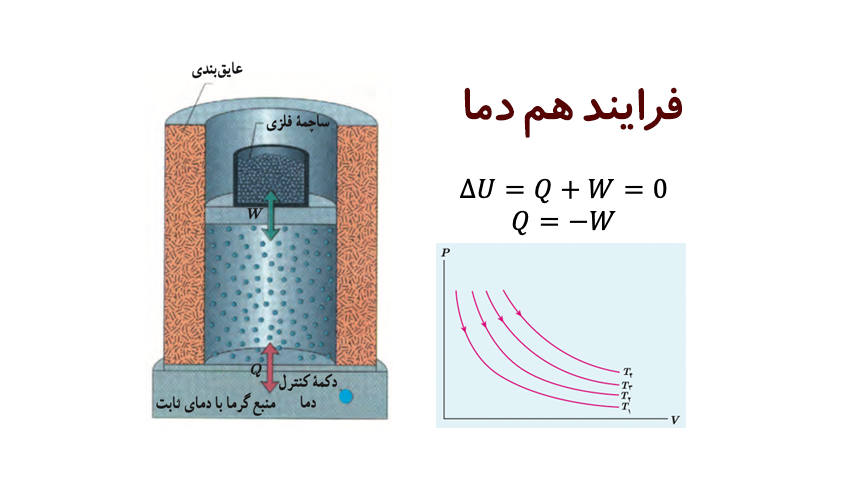
فرایند هم دما
تغییر انرژی درونی، گرما و کار
در فرایند هم دما ، دمای گاز تغییر نمی کند. بنابراین برای گاز آرمانی که انرژی درونی آن فقط تابعی از دماست، تغییر انرژی درونی صفر است.
با استفاده از قانون اول ترمودینامیک، می توان رابطه بین کار و گرما در فرایند هم دما را به صورت زیر نوشت.
نمودار های فرایند هم دما
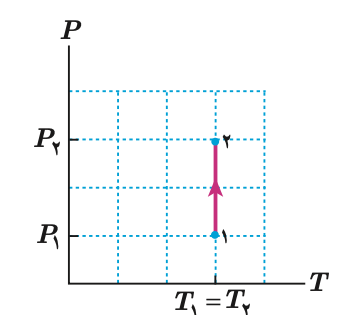
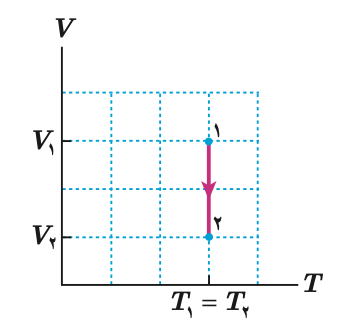
در تراکم هم دما، کار انجام شده روی گاز مثبت است. در نتیجه طبق رابطه بالا، Q منفی می شود. یعنی در تراکم هم دما، گاز گرما از دست می دهد. با کاهش حجم گاز، افزایش فشار خواهیم داشت. نمودار P-T این فرایند برای حالت تراکم به صورت زیر خواهد بود.
برای رسم نمودار P-V این فرایند به مثال زیر توجه کنید.
مثال ۱: گازی آرمانی را در دمای ثابت از حالت اولیه V1=4L و P1=1atm تا حالت نهایی با حجم V2=1L متراکم می کنیم.
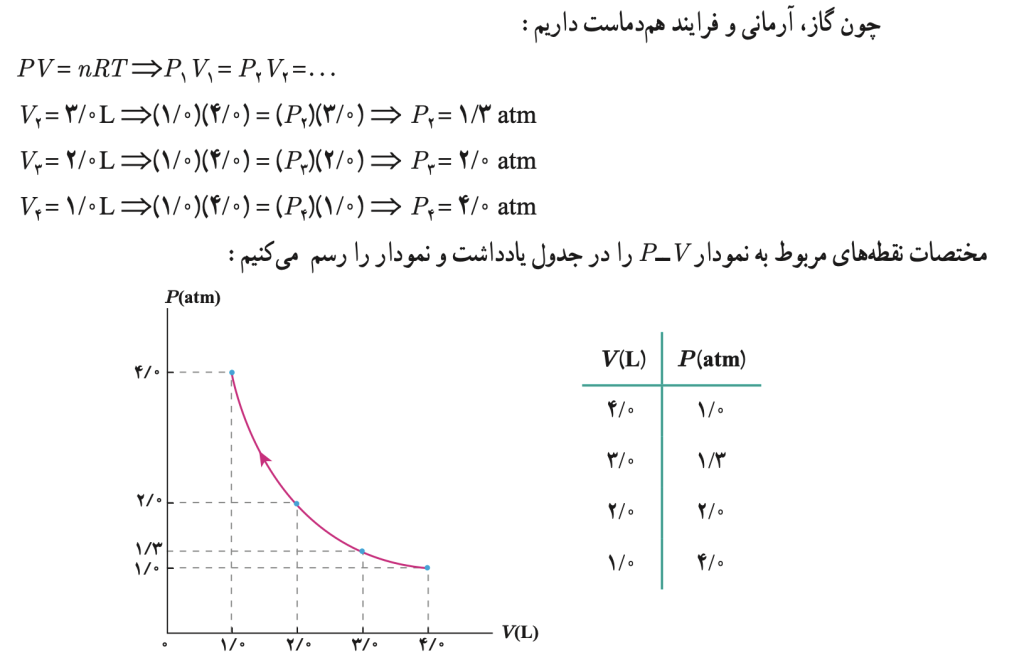
الف) در طی این فرایند، فشار گاز را برای هر یک از حجم های ۳L و ۲L و ۱L حساب کنید و نمودار P-V را با استفاده از روش نقطه یابی و معلوم بودن مختصات هر نقطه رسم کنید.
ب) اگر مساحت سطح زیر این نمودار ۵۵۰۰ ژول باشد،Q و W در این فرایند چقدر است؟
پاسخ: الف)
ب) چون گاز متراکم می شود کار و گرما به صورت زیر حساب می شوند.
مثال ها
مثال ۲: انتهای یک سرنگ حاوی هوا را مسدود و آن را وارد حجم بزرگی از آب کنید. پس از مدتی، پیستون سرنگ را به آرامی بفشارید. هوای درون سرنگ چه فرایندی را طی میکند؟
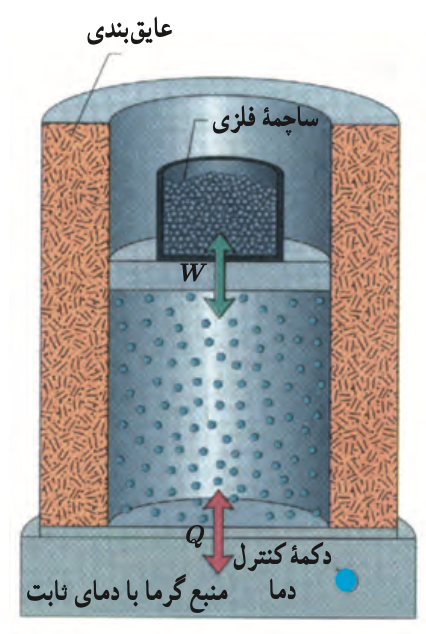
پاسخ: وقتی سرنگ حاوی هوا را در آب می اندازیم و مدتی صبر میکنیم، هوای درون سرنگ با آب هم دما می شود. از این پس، هوای درون سرنگ در ارتباط با منبع گرما (حجم بزرگ آب) قرار دارد. و چون به صورت خیلی آهسته پیستون را فشار می دهیم، افزایش فشار و کاهش حجم در فرایند هم دما خواهیم داشت.
چون دمای دستگاه همان دمای منبع گرما با قی می ماند. در هر مرحله کوچک این فرایند، دما ابتدا کمی زیاد می شود ولی این افزایش دما با دادن گرما به آب جبران می شود تا اینکه هوا دوباره با آب هم دما شود.
دقت داشته باشید که در این فرایند،گاز با محیط تبادل گرما می کند بی آنکه دمایش تغییر کند.در واقع اهمیت فرایند هم دما در تبدیل کامل کار و گرما به یکدیگر است. وقتی محیط روی دستگاه کار انجام دهد، به همان اندازه دستگاه به محیط گرما می دهد.
الف) نشان دهید:
ب) در یک تغییر حجم معین، اندازه کار انجام شده در کدام فرایند بیشتر است؟
پاسخ: الف) با توجه به معادله حالت خواهیم داشت.
اگر خطی عمود بر محور V رسم کنیم، روی این خط مقدار داخل پرانتز، برای هر ۴ حالت یکسان است.چون V یک مقدار خاص دارد. بنابراین نموداری که روی این خط عمود، فشار بیشتری دارد (یعنی بالاترین نمودار) دمای بیشتری دارد.
ب) اندازه کار به مساحت سطح زیر نمودار P-V مربوط است. پس نمودار بالایی مساحت زیر نمودار بیشتری دارد، یعنی خواهیم داشت.
دقت داشته باشید چون فرایند انبساطی است، کار مقداری منفی دارد.
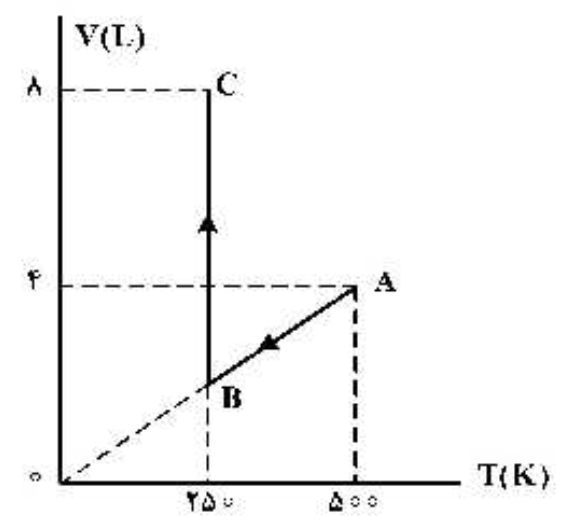
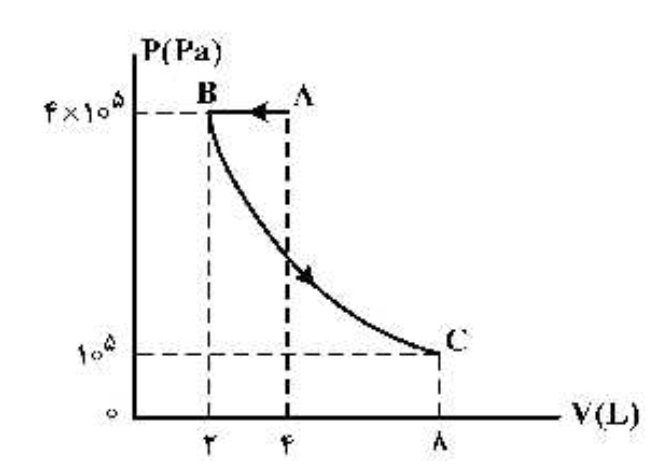
پاسخ: فرایند AB تراکم هم فشار است یعنی در نمودار جدید باید عمود بر محور P باشد. و فرایند BC انبساط هم دما است که در نمودار P-V به صورت منحنی است. برای محاسبات هم نیز از معادله حالت استفاده میکنیم تا فشار را در نقاط مختلف حساب کنیم.
در نتیجه نمودار P-V این فرایند به صورت زیر می شود.
برای طرح مثال های بیشتر نیاز داریم تا فرایند های دیگر را نیز بیاموزیم. چون که در مثال ها چند فرایند مختلف داریم. برای مشاهده مثال های بیشتر به این مطلب مراجعه کنید.
ویدیو آموزشی
در این ویدیو آموزشی به بررسی روابط و نمودار های فرایند هم دما توسط استاد مصطفی کبیری پرداخته می شود.
مشاهده در یوتیوب | مشاهده در آپارات