در یکی از آموزش های فیزیکفا، به گرما و دمای تعادل بین دو یا چند جسم که با یکدیگر تبادل گرما داشتند، پرداختیم. و نحوه محاسبه دمای تعادل را با مثال ها و تمرین هایی شرح دادیم. اما در این آموزش به چگونگی محاسبه دمای تعادل در صورت تغییر فاز می پردازیم. یعنی زمانی که ماده ذوب می شود یا برعکس آن منجمد می شود یا حالت هایی که تبخیر و میعان صورت می گیرد.
گرمای نهان ذوب
اگر به جسم جامدی گرما دهیم، دمای آن افزایش می یابد. اگر عمل گرما دادن را برای جامدهای خالص و بلورین ادامه دهیم، وقتی دمای جسم به مقدار مشخصی برسد، افزایش دما متوقف می شود. و دما ثابت باقی می ماند. این دما را که در آن جسم شروع به ذوب شدن می کند، نقطه ذوب یا دمای گذار جامد به مایع می نامند. که به جنس جسم و فشار وارد بر آن بستگی دارد. بر خلاف جامدهای بلورین، جامدهای بی شکل مانند شیشه و جامدهای ناخالص مانند قیر، نقطه ذوب معینی ندارند و در گستره ای از دما به تدریج ذوب می شوند.
انجماد یک مایع و تبدیل آن به یک جامد، عکس فرایند ذوب شدن است. در اینجا نیز تغییر حالت بدون تغییر دما رخ می دهد. گرمای منتقل شده برای تغییر حالت جسم از جامد به مایع یا از مایع به جامد، با جرم جسم نسبت مستقیم دارد. نسبت این گرما به جرم جسم را گرمای نهان ویژه ذوب می گویند. که به اختصار آن را گرمای نهان ذوب می نامیم و رابطه آن را در زیر مشاهده می کنید:
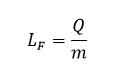 گرمای نهان ذوب به جنس جسم بستگی دارد و یکای آن در SI طول بر کیلوگرم (J/Kg) است.
گرمای نهان ذوب به جنس جسم بستگی دارد و یکای آن در SI طول بر کیلوگرم (J/Kg) است.
بنابراین برای وقتی جسم جامدی گرما می گیرد و ذوب می شود، گرما از رابطه زیر بدست می آید:
![]() و وقتی مایعی گرما از دست می دهد و منجمد می شود، گرما از رابطه زیر بدست می آید:
و وقتی مایعی گرما از دست می دهد و منجمد می شود، گرما از رابطه زیر بدست می آید:
![]() البته در روش حلی که ما برای شما ارائه می دهیم، علامت مثبت و منفی مهم نیست و فقط مقدار گرمای گرفته شده یا ازدست داده شده مهم است.
البته در روش حلی که ما برای شما ارائه می دهیم، علامت مثبت و منفی مهم نیست و فقط مقدار گرمای گرفته شده یا ازدست داده شده مهم است.
ویدیو گرمای نهان ذوب
در ویدیو زیر با مفاهیم ذوب، انجماد، تبخیر، میعان، تصعید و چگالش آشنا می شوید. فرمول گرمای نهان ذوب و مثال های حل شده و کاربرد آن در محاسبه دمای تعادل را در ویدیو زیر می آموزید. ویدیو توسط استاد مصطفی کبیری آماده شده است.
مشاهده در یوتیوب | مشاهده در آپارات
گرمای نهان تبخیر
وقتی به مایعی گرما می دهیم در دمای مشخصی حباب های گاز از درون مایع به بالا می آیند که نشانه جوشیدن است. در این حالت دیگر تغییر دما رخ نمی دهد و مایع تبدیل به گاز می شود که به این فرایند، تبخیر می گوییم. البته تبخیر در هر دمایی رخ می دهد که به آن تبخیر سطحی می گوییم و در این حالت نیاز نیست مایع به نقطه جوش برسد. بر عکس این فرایند میعان نام دارد.
نسبت گرمای منتقل شده برای تبخیر هر مایع به جرم مایع بخار شده را گرمای نهان تبخیر می نامیم که از رابطه زیر بدست می آید:
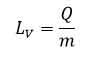 گرمای نهان تبخیر به جنس مایع بستگی دارد و یکای آن در SI طول بر کیلوگرم (J/Kg) است.
گرمای نهان تبخیر به جنس مایع بستگی دارد و یکای آن در SI طول بر کیلوگرم (J/Kg) است.
بنابراین برای وقتی مایعی گرما می گیرد و بخار می شود، گرما از رابطه زیر بدست می آید:
![]() و وقتی گاز گرما از دست می دهد و تبدیل به مایع می شود، گرما از رابطه زیر بدست می آید:
و وقتی گاز گرما از دست می دهد و تبدیل به مایع می شود، گرما از رابطه زیر بدست می آید:
البته در روش حلی که ما برای شما ارائه می دهیم، علامت مثبت و منفی مهم نیست و فقط مقدار گرمای گرفته شده یا ازدست داده شده مهم است.
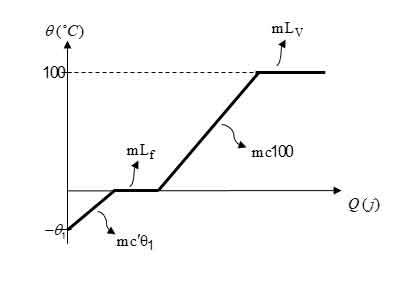
نمودار زیر برای اینکه درک صحیحی پیدا کنید که چه زمانی باید از روابط بالا استفاده کرد به شما نشان می دهد:
ویدیو گرمای نهان تبخیر
در ویدیو زیر با مفاهیم گرمای نهان تبخیر و میعان و مثال های حل شده و کاربرد آن در محاسبه دمای تعادل آشنا می شوید. ویدیو توسط استاد مصطفی کبیری آماده شده است.
مشاهده در یوتیوب | مشاهده در آپارات
روش حل مساله های محاسبه گرما و دمای تعادل با در نظر گرفتن تغییر حالت ماده
برای حل مساله های این قسمت و محاسبه گرما و دمای تعادل، ما روش خاصی را در نظر گرفته ایم که در آن گرمای گرفته شده و گرمای از دست داده شده، مهم است. برای انجام این روش حل به نکات زیر توجه کنید:
- ابتدا باید دید چه ماده ای گرما از دست می دهد و چه ماده ای گرما می گیرد. ماده ای که دمای بالاتری دارد گرما از دست می دهد و ماده ای که دمای کمتری دارد گرما می گیرد.
- هنگامی که آب و یخ در فشار یک اتمسفر (فشار سطح دریای آزاد) به تعادل می رسند یعنی پس از رسیدن به تعادل هم یخ و هم آب داشته باشیم، دمای تعادل صفر درجه سلسیوس است.
- آب در فشار یک اتمسفر در دمکای ۱۰۰ درجه سلسیوس تبخیر می شود و بخار آب در همین دما به آب تبدیل می شود.
- برای حل سوالات،و محاسبه گرما و دمای تعادل ، یافتن محصول نهایی بسیار مهم است. یا باید در متن سوال محصول نهایی و دمایش را مشخص کرد و یا اینکه یک آزمایش ساده انجام دهیم. یعنی رساندن ماده به نقاط مرزی تغییر حالت و محاسبه گرمای مورد نیاز. این آزمایش در حل مثال ها و تمرین ها بیشتر توضیح داده شده و راحت تر فهمیده می شود.
- در صورتی که ماده مورد نظر سوال، آب باشد و تغییر حالت های آن بررسی شود می توان در صورتی که ثابت های گرمای ویژه و گرمای نهان ذوب و تبخیر بر حسب اعداد زیر باشند، می توان از تابت های داخل کادر استفاده کرد تا محاسبات ساده شود. در ۹۰ درصد سوالات این اعداد داده می شوند.
ویدیو روش حل مساله
نکات گفته شده در بالا، در روش حل مساله های دمای تعادل وقتی تغییر فاز داریم، را در ویدیوی زیر ببینید. و کاربرد آن ها در حل مثال ها را یاد بگیرید.
مشاهده در یوتیوب | مشاهده در آپارات
مثال های حل شده محاسبه گرما و دمای تعادل
مثال ۱: یک گلوله فلزی به جرم ۸۰۰ گرم و دمای ۴۲ درجه سلسیوس را روی قطعه یخ بزرگ صفر درجه سلسیوس قرار می دهیم. پس از برقراری تعادل، جرم یخ ذوب شده چند گرم است؟ (گرمای ویژه فلز ۰٫۲J/gC و گرمای نهان ذوب یخ ۳۳۶J/gاست.)
حل مثال ۱: در این مساله دو جسم داریم. ۸۰۰ گرم فلز با دمای ۴۲ و قطعه یخی با دمای صفر . با توجه به دمای فلز می فهمیم، فلز گرما از دست می دهد و یخ گرما می گیرد تا بخشی از آن ذوب شود و چون یخ بزرگ است پس در نهایت مقداری آب و یخ خواهیم داشت که حتما دمای انها صفر خواهد بود. پس محصول نهایی فلز با دمای صفر و مقداری آب صفر و باقی مانده یخ صفر خواهد بود.
مقدار گرمایی که فلز از دست می دهد تا به دمای صفر برسد برابر است با مقدار گرمایی که بخشی از یخ می گیرد تا تبدیل به آب صفر شود. یعنی می توان نوشت :
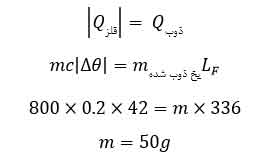 در نتیجه ۵۰ گرم از یخ ذوب دشه و تبدیل به آب صفر می شود.
در نتیجه ۵۰ گرم از یخ ذوب دشه و تبدیل به آب صفر می شود.
مثال ۲: ۲۰۰ گرم آب صفر را روی ۱۰۰ گرم یخ منفی ۱۲ درجه سلسیوس می ریزیم. محصول نهایی را مشخص کنید.
حل مثال ۲: با توجه به اینکه دمای آب صفر بیشتر است، پس آب صفر گرما ازدست می دهد و یخ می زند. اما نمی توان محصول نهایی را مشخص کرد. بنابراین باید آزمایش ساده ای را انجام دهیم. پس فرض های زیر را انجام می دهیم و هر یک از مواد را به اولین شرایط مرزی که می رسد، می بریم و گرما های انها را حساب می کنیم. و همچنین ثابت ها را بر اساس کادر بالا قرار می دهیم. مطابق زیر :
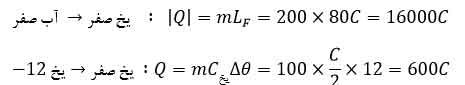 با توجه به اعداد بالا مقدار گرمای لازم برای اینکه کل یخ منفی ۱۲ به یخ صفر تبدیل شود (۶۰۰C) تامین خواهد شد. و چون هر دو به صفر درجه می رسند پس دمای تعادل صفر است. پس می توان نتیجه گرفت که کل آب صفر یخ نمی زند و فقط بخشی از آن به اندازه گرمای (۶۰۰C) یخ می زند. یعنی :
با توجه به اعداد بالا مقدار گرمای لازم برای اینکه کل یخ منفی ۱۲ به یخ صفر تبدیل شود (۶۰۰C) تامین خواهد شد. و چون هر دو به صفر درجه می رسند پس دمای تعادل صفر است. پس می توان نتیجه گرفت که کل آب صفر یخ نمی زند و فقط بخشی از آن به اندازه گرمای (۶۰۰C) یخ می زند. یعنی :
پس محصول نهایی ۱۰۷٫۵ گرم یخ صفر و ۱۹۲٫۵ گرم آب صفر خواهد بود.
همانطوری که مشاهده کردید در سوالاتی که محصول نهایی مشخص نیست با یک آزمایش ساده، محصول نهایی مشخص می شود. مقایسه دو جمله آزمایش بسیار مهم است.
ویدیو حل تست های کنکور سراسری ۹۷ و ۹۸
قبل از اینکه تمرین های زیر را حل کنید و پاسخ آن ها را ببینید توصیه می کنیم ویدیوی آموزشی زیر از این محث را حتما تماشا کنید تا نسبت به این روش تسلط کافی پیدا کنید:
مشاهده در یوتیوب | مشاهده در آپارات
تمرین های گرما و دمای تعادل با در نظر گرفتن تغییر حالت ماده
تمرین ۱: حداقل چند گرم یخ منفی ۲۰ درجه سلسیوس را در داخل ۲۰۰ گرم آب صفر درجه بیندازیم تا تمام آب یخ ببندد؟
تمرین ۲: ۶٫۴ کیلوگرم یخ منفی ۱۰ درجه سلسیوس را در استخر پر از آب صفر درجه می اندازیم، پس از برقراری تعادل وزن یخ چند کیلوگرم می شود؟
تمرین ۳: قطعه یخی به جرم m و دمای صفر درجه ی سلسیوس را درون همان جرم آب ۹۰ درجه ی سلسیوس می اندازیم. اگر از اتلاف گرما صرف نظر کنیم، دمای تعادل چند درجه ی سلسیوس خواهد شد؟
تمرین ۴: درون ظرفی ۴۰۰ گرم مخلوط آب و یخ در دمای صفر درجه سلسیوس در حالت تعادل قرار دارد. اگر فلزی به جرم ۲۰۰ گرم گرمای ویژه ۸۴۰J/KgC و دمای ۱۰۵ درجه سلسیوس را داخل آب بیندازیم، بعد از برقراری تعادل، دمای آب به ۵ درجه سلسیوس می رسد. جرم یخ چند گرم بوده است ؟
تمرین ۵: درون ۲ کیلوگرم آب ۴۰ درجه سلسیوس مقداری یخ منفی ۵ درجه سلسیوس می اندازیم. اگر این آب ۲۹۴ کیلوژول گرما از دست بدهد تا سیستم به دمای تعادل برسد، جرم یخ چند گرم بوده است؟


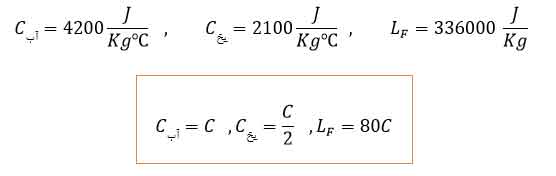
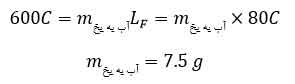

6 دیدگاه دربارهٔ «گرما و دمای تعادل با در نظر گرفتن تغییر حالت ماده»
اززحماتتون بسیارممنویم
عالی توضیح دادین
خواهش می کنم
عالی
خیلی استفاده کردم
ممنون
سپاس